sexta-feira, 21 de setembro de 2007
Atividades de física ( escalas termometricas)
r:Tc = tf-32
5 9
Tc = 50 - 32
5 9
Tc = 18
5 9
Tc= 2
5
Tc=2.5 = 10ºc
2: Trasforme 47 ºc em ºk.
T = Tc+ 273
T = 47 + 273 = T = 320k
3: Trasforme 41 ºf ºk
R: Tf-32 = tk- 273
9 5
41-32 = tk-273
9 5
9 = Tk-273
9 5
Tk-273 = 5.1
Tk = 273+ 5 = Tk =278k
quinta-feira, 20 de setembro de 2007
Escalas Termométricas
Escalas Termometricas sao escalas que permitem "medir" certa temperatura, relacionando-a, geralmente,com altura. As escalas mais conhecidas sao o Celsius, Fahrenheit e Kelvin!
COMO CRIAR ESCALAS TERMOMÉTRICAS
Para construir uma escala devemos primeiro escolher uma grandeza termomátrica, ou seja, qualquer grandeza que varie com a temperatura. São exemplos de grandezas termométricas o comprimento de uma coluna de mercúrio, o tamanho de uma barra de ferro, a pressão exercida por um gás num recipiente de volume constante, a resistência elétrica de um fio, entre outras. A relação entre a grandeza termométrica e a temperatura deve ser tal que cada valorda grandeza corresponda a uma única temperatura. A medida da temperatura de um corpo será feita indiretamente, pelo efeito provocado na grandeza termométrica quando estiver em equilíbrio térmico com o corpo.
- Os procedimentos são:
- Escolhemos a substância e a grandeza termométrica que varia linearmente com a temperatura. Por exemplo, o álcool colorizado (substância termométrica) colocado em um reservatório (bulbo) ligado a um tubo capilar de vidro; o comprimento atingido pela coluna de álcool no tubo capilar é a (grandeza térmica). Essa grandeza - comprimento da coluna de álcool - varia linearmente com a temperatura.
- Esse dispositico é colocado em contato com dois estados térmicos diferentes, denominados pontos físicos. Os mais utilizados são a ebulição da água (100°C) e a fusão da água (0°C), ambos sob pressão de 1 atm.
- É feita a marcação da altura, no momento que a água estava em fusão, dando a esse ponto a altura h1 e um número, o T1. O momento da ebulição da água é marcado por outro ponto na escala, o h2 e por outro numero, T2. O intervalo entre dois pontos físicos (h2-h1) é dividido por (T1-T2) e resulta em partes iguais e unitárias. Cada unidade recebe o nome de grau da escala.
PRINCIPAIS ESCALAS E SUAS CORREPONDÊNCIAS
As escalas mais famosas são a Celsius, Kelvin e Farenheit.
- PONTOS DE FUSAO E EBULIÇÃO DA ÁGUA
A água em pressao de 1 atm, congela a esses valores.
0º C
-32Fº
173K
100ºC
212ºF
373 K
Calorimetria
A forma de energia denominada calor só pode ser concebida quando conjugada com uma permuta de energia, pelo que o termo calor está sempre associada a fluxo de calor. A palavra calorímetro é usada para designar um instrumento utilizado na medição de calor envolvido numa mudança de estado de um sistema. Tal pode envolver uma mudança de fase, de temperatura, de pressão, de volume, de composição química ou qualquer outra propriedade associada com trocas de calor.
Tipos de Calorímetros
Calorímetros Isotérmicos
São aqueles em que idealmente não há variação de temperatura durante a experiência.
Calorímetros Isoperibol
Um calorímetro isoperibol é aquele em que a temperatura do Meio é mantida constante, independentemente da temperatura do calorímetro propriamente dito, embora se tente que as diferenças de temperatura não sejam elevadas. Conseqüentemente, as trocas de calor entre o vaso calorimétrico e o Meio existem deliberadamente e, sendo devidamente controladas, a quantidade de calor permutado entre aqueles dois meios é conhecida e proporcional à diferença das respectivas temperaturas.
Calorímetros de Varredura Exploratória ou Calorimetria Exploratória Diferencial
Neste tipo de calorímetro, a temperatura no sistema calorimétrico ou a temperatura no meio podem variar de forma linear ou isotérmica e programada ao longo do tempo.
Principais grandezas estudadas
Calorimetria
Não podemos começar a falar sobre o estudo da calorimetria sem antes definirmos o que é "calor".
Calor: É o agente responsável pelas variações de temperatura, as mudanças no estado de agregação dos corpos (vaporização dos líquidos, fusão dos sólidos, etc.) e as dilatações e contrações que ocorrem em função das variações do estado térmico dos corpos. Agora definiremos uma outra grandeza física muito importante, a capacidade térmica, e apresentaremos sua fórmula e sua unidade de medida no S.I.
Capacidade Térmica (C): Grandeza Física que permite prever dentro de um dado conjunto de corpos, onde cada um cede ou recebe a mesma quantidade de calor, qual deles estará mais quente ou mais frio, ao completar a troca de calor.

- C: capacidade térmica do corpo.
- Q: quantidade de calor trocada pelo corpo.
- Δθ: variação de temperatura do corpo.
A unidade de capacidade térmica no S.I. é o J/K.
Calor Específico (c): Grandeza Física que permite prever dentro de um dado conjunto de amostras de diversos materiais, todas de mesma massa, qual delas recebendo ou cedendo a mesma quantidade de calor, estará mais quente ou mais fria, ao completar a troca de calor.
A unidade usual para determinar o calor específico é
cal / g0C e no S.I. é o J/kgK.
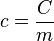
- c: calor específico de um dado material.
- C: capacidade térmica da amostra deste material.
- M: massa da amostra deste material.
Uma caloria (1 cal): é a quantidade de calor necessária para aquecer, sob pressão normal, 1,0 g de água de 14,50ca15,50c.
Função Fundamental da Calorimetria (Quantidade de Calor Sensível)
Ocorre mudança de temperatura nas substâncias.
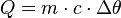
mais conhecido como Quimicão ou mc deltateta
- Q>0 (o corpo recebe calor)
0" src="http://upload.wikimedia.org/math/7/2/1/721f6b16f0d2400e9d4c9a2c4d05e249.png"> (o corpo se aquece).
- Q<0 class="tex" alt="\rightarrow\Delta\theta <0" src="http://upload.wikimedia.org/math/3/9/4/3943d99b42c0dddd734bc149a7168a8f.png">(o corpo se esfria).
Quantidade de Calor Latente
Ocorre mudança de estado nas substâncias.

Propriedades Envolvidas nas trocas de Calor (Princípios da Calorimetria)
- Princípios de transformações inversas: a quantidade de calor que um corpo recebe é igual, em módulo, à quantidade de calor que um corpo cede ao voltar, pelo mesmo processo, à situação inicial.
- Princípio do Equilíbrio Térmico: quando vários corpos inicialmente a temperaturas diferentes trocam calor entre si, e só entre si, observamos que alguns perdem enquanto outros recebem calor, de tal maneira que decorrido um certo tempo, todos estacionam numa mesma temperatura, chamada temperatura de equilíbrio térmico.
- Princípio da Igualdade das Trocas de Calor: quando vários corpos trocam calor apenas, entre si, a soma das quantidades de calor que alguns cedem é igual, em módulo, à soma das quantidades de calor que os restantes recebem.
Q1 + Q2 + ... + Qn = 0
Termodinâmica
É bastante conhecido o fato de que uma substância é constituída de um conjunto de partículas denominadas de moléculas. As propriedades de uma substância dependem, naturalmente, do comportamento destas partículas.
A partir de uma visão macroscópica para o estudo do sistema, que não requer o conhecimento do comportamento individual destas partículas, desenvolveu-se a chamada termodinâmica clássica. Ela permite abordar de uma maneira fácil e direta a solução de nossos problemas. Uma abordagem mais elaborada, baseada no comportamento médio de grandes grupos de partículas, é chamada de termodinâmica estatística.
Processos
Sempre que uma ou mais propriedades de um sistema varia, diz-se que ocorreu uma mudança de estado. O caminho através de sucessivos estados pelo qual passa o sistema é definido como processo. Um processo de quase-equilíbrio (quasi-estático) é aquele em que o desvio do equilíbrio termodinâmico é infinitesimal, e todos os estados pelo qual o sistema passa pode ser considerado como estados de equilíbrio. Muitos processos reais podem ser aproximados com precisão pelo processo de quase-equilíbrio.
Equilíbrio
Por outro lado, se um processo evolui muito rapidamente e o sistema não esteve em equilíbrio durante nenhum instante durante a mudança de estado, este é um processo de não-equilíbrio. Na termodinâmica clássica a descrição destes processos fica limitada ao que havia antes e depois de restabelecido o equilíbrio, sendo esta incapaz de especificar os estados intermediários pelo qual passou o sistema. Uma abordagem mais eficiente destes processos é feita através da termodinâmica do não equilíbrio ( a abordagem não é unaminidade entre os estudiosos da área, alguns preferem outros tipos).
Termodinâmica
A termodinâmica permite determinar a direção na qual vários processos físicos e químicos irão ocorrer. Também permite determinar as relações entre as diversas propriedades de uma substância. Contudo ela não trabalha com modelos da microestrutura da substância, e não é capaz de fornecer detalhes dela, mas uma vez que alguns dados sejam conhecidos, através do método da termodinâmica clássica, outras propriedades podem ser determinadas.
Leis da Termodinâmica
A termodinâmica é baseada em leis estabelecidas experimentalmente:
- A Lei Zero da Termodinâmica determina que, quando dois corpos têm igualdade de temperatura com um terceiro corpo, eles têm igualdade de temperatura entre si. Esta lei é a base para a medição de temperatura.
- A Primeira Lei da Termodinâmica fornece o aspecto quantitativo de processos de conversão de energia. É o princípio da conservação da energia e da conservação da massa, agora familiar, : "A energia do Universo é constante".
- A Segunda Lei da Termodinâmica determina o aspecto qualitativo de processos em sistemas físicos, isto é, os processos ocorrem numa certa direção mas não podem ocorrer na direção oposta. Enunciada por Clausius da seguinte maneira: "A entropia do Universo tende a um máximo".
- A Terceira Lei da Termodinâmica estabelece um ponto de referência absoluto para a determinação da entropia, representado pelo estado derradeiro de ordem molecular máxima e mínima energia. Enunciada como "A entropia de uma substância cristalina pura na temperatura zero absoluto é zero". É extremamente útil na análise termodinâmica das reações químicas, como a combustão, por exemplo.